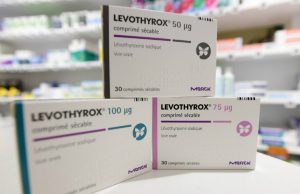
«Di recente – ha scritto l’eurodeputata – numerosi scandali legati ai farmaci si sono verificati in Francia. L’ultimo in ordine di tempo, del quale le responsabilità non sono state ancora stabilite, coinvolge l’industria Merck e la nuova formula della loro molecola Levothyrox (l’Eutirox in Italia, ndr). La sua commercializzazione ha provocato un’ondata di effetti collaterali, ancora oggi non spiegati, tra i pazienti che assumono il medicinale». La vicenda era stata raccontata da FarmaciaVirtuale.it: in particolare il fatto che numerosi cittadini transalpini avevano deciso di varcare la frontiera e recarsi in Italia per poter acquistare la vecchia formula del farmaco. «La commissione – aggiunge Montel – pensa che il sistema di farmacovigilanza adottato nell’Ue sia efficace, tenendo conto che gli Stati membri dispongono anch’essi di sistemi nazionali? Si prevedono modifiche nel funzionamento? Non sarebbe utile riflettere su un sistema unico di supervisione indipendente a livello globale, gestito dall’Organizzazione Mondiale della Sanità?».
«Per ciò che riguarda l’efficacia del sistema europeo di farmacovigilanza – ha risposto Andriukaitis – è bene sottolineare che i farmaci in circolazione nell’Ue sono sottoposti ad uno stretto monitoraggio, e che le regole per i titolari di autorizzazione all’immissione in commercio sono fissate a livello comunitario e, pertanto, armonizzate». Il che fa di quello europeo, secondo il commissario, «uno dei sistemi più perfezionati e completi al mondo, nonché uno strumento solido e trasparente per garantire un alto livello di protezione della salute pubblica». Sulla questione del Levothyrox, poi, Andriukaitis ha ricordato che «nel quadro del cambiamento di una formula, le autorità nazionali competenti chiedono il parere del comitato di valutazione dei rischi in materia di farmacovigilanza dell’EMA (PRAC) in riferimento ai problemi di sicurezza potenziali. Sulla base delle informazioni disponibili, il PRAC ha ritenuto che non ci fossero differenze negli effetti collaterali osservati con la vecchia e con la nuova formula». In ogni caso, «è stato consigliato di procedere ad una stretta sorveglianza nel periodo di transizione sull’insieme dei pazienti». Infine, il commissario si è detto contrario all’ipotesi di una farmacovigilanza mondiale.
[Se non vuoi perdere tutte le novità iscriviti gratis alla newsletter di FarmaciaVirtuale.it. Arriva nella tua casella email alle 7 del mattino. Apri questo link]
Non perdere gli aggiornamenti sul mondo della farmacia
Riceverai le novità sui principali fatti di attualità.
Puoi annullare l'iscrizione con un click. Non condivideremo mai il tuo indirizzo email con terzi.