Il 14 maggio 2021 il ministero della Salute ha emanato la circolare n. 21675 in materia di uso dei test molecolare e antigenico su saliva ad uso professionale per la diagnosi di infezione da Sars-Cov-2. A richiamare alcune disposizioni è la Federazione degli ordini dei farmacisti (Fofi), la quale precisa che «nel suddetto documento si rammenta, preliminarmente, che il test molecolare su campione nasofaringeo e orofaringeo rappresenta il gold standard internazionale per la diagnosi di Covid-19 in termini di sensibilità e specificità. In caso di mancata e pronta disponibilità di test molecolari o in condizioni d’urgenza determinate dalla necessità di prendere decisioni di sanità pubblica in tempi rapidi, si può ricorrere ai test antigenici sempre su campione nasofaringeo e orofaringeo, quali i test antigenici da eseguire in laboratorio, oppure ai test antigenici rapidi con lettura in fluorescenza o basati su microfluidica con lettura in fluorescenza, che rispondano alle caratteristiche di sensibilità e specificità minime (sensibilità ≥ 80% e specificità ≥ 97%, con un requisito di sensibilità più stringente (≥90%) in contesti a bassa incidenza)».
[Se non vuoi perdere tutte le novità iscriviti gratis alla newsletter di FarmaciaVirtuale.it. Arriva nella tua casella email alle 7 del mattino. Apri questo link]
Il via libera del Ministero ai test salivari molecolari
In merito al via libera del ministero della Salute ai test salivari molecolari, la Fofi evidenzia che «al riguardo, vengono poste però alcune limitazioni “perché la sensibilità diminuisce dopo i primi 5 giorni dall’inizio dei sintomi” e perché “il campione di saliva può essere considerato un’opzione per il rilevamento dell’infezione da Sars-CoV-2 qualora non sia possibile ottenere tamponi oro/nasofaringei”». La Fofi aggiunge poi che «il Ministero, nell’indicare quando usare il test salivare molecolare, evidenzia che il campione di saliva “può essere considerato un’opzione per il rilevamento dell’infezione da Sars-Cov-2 in individui asintomatici sottoposti a screening ripetuti per motivi professionali o di altro tipo, per aumentare l’accettabilità di test ripetuti, in particolare: se vengono sottoposti a screening individui molto anziani o disabili e in caso di carenza di tamponi”».
Le modalità di raccolta del campione
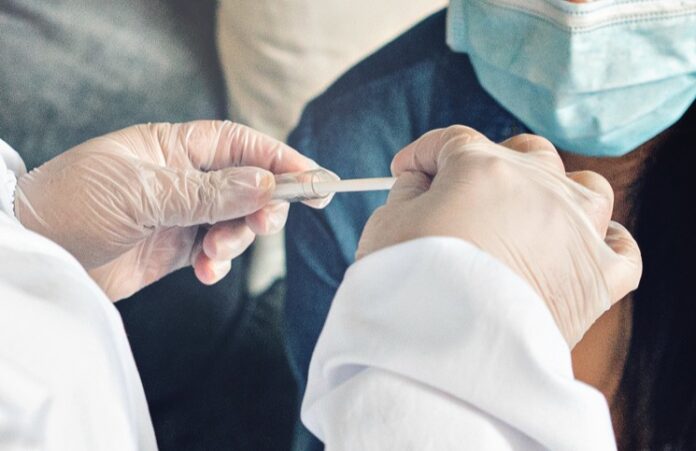
Quanto alla raccolta del campione, la Fofi – citando la nota del ministero della Salute – evidenzia che «l’uso della saliva “prevede un metodo di raccolta non invasivo, tuttavia, la corretta raccolta del campione salivare è un passaggio cruciale. I campioni di saliva possono essere eterogenei (saliva orale, saliva orofaringea posteriore) e le diverse tecniche e sedi di raccolta possono avere un impatto sulla sensibilità del metodo. Inoltre, i campioni di saliva possono essere mucosi e viscosi, determinando difficoltà di lavorazione con i metodi e le attrezzature automatizzate di estrazione dell’Rna o di estrazione/amplificazione esistenti”».
L’utilità dei test salivari molecolari
Proprio sulla saliva il ministero della Salute puntualizza che «è stata valutata “come possibile substrato per i test antigenici basati su strumentazione automatica di laboratorio, con lettura in chemiluminescenza. Al momento, il repertorio disponibile di tali test marcati Ce-Ivd per la matrice salivare è limitato, ma è in corso di ampliamento. Il confronto con il test molecolare indica per la saliva una sensibilità simile a quella osservata per il tampone nasofaringeo”». Inoltre «i test salivari molecolari “possono rappresentare uno strumento utile per il monitoraggio e controllo dell’infezione da Sars-Cov-2 in ambito scolastico. Alcuni studi pubblicati nel 2020 hanno rilevato sensibilità comprese tra il 53 e il 73%”». Un ultimo riferimento al sistema di sorveglianza nazionale Covid-19, secondo cui «“i test molecolari su campione salivare – specifica il Ministero – dovranno essere segnalati nel sistema di sorveglianza” e, ai fini della tracciabilità, che “gli esiti dei test molecolari su campione salivare, anche se effettuati da laboratori, strutture e professionisti privati accreditati dalle Regioni, devono essere inseriti nel sistema informativo regionale di riferimento”».
Documenti allegati
Non perdere gli aggiornamenti sul mondo della farmacia
Riceverai le novità sui principali fatti di attualità.
Puoi annullare l'iscrizione con un click. Non condivideremo mai il tuo indirizzo email con terzi.



